一、前言
在众多环境污染中,重金属由于自身不能被自然降解,进而易通过食物链进入人体,严重危害人类健康,因此在水体中的污染越来越引起人们的注意。铅、镉、铜及其化合物因广泛应用于采矿、冶炼、电子、电镀石油、肥料制造等行业,已成为污水中的重要污染源而备受人们的关注,在环保、卫生、食品等部门世界各国均有严格的法规限制其允许量。
活性炭作为一种非极性吸附剂,来源丰富,是目前废水处理中应用广的吸附剂之一。它具有良好的吸附性能和稳定的化学性质,可以耐强酸、强碱,能经受水浸、高温高压作用,同时还可以活化再生。吸附法处理废水的经济应用主要取决于活性炭制备材料的费用,因此低能耗的材质选择用于制备活性炭成为目前研究的热点。在此项工作中。波涛活性炭厂家研究了自制的石油焦活性炭对重金属铜铅镉离子的吸附去除能力,测定了不同条件对活性炭吸附溶液中铅镉铜离子的影响,为处理微量重金属废水作出有意义的探索。现将实验结果分析如下:
一、pH对活性炭吸附铅镉离子的影响
活性炭表面各类含氧基团、官能团,主要以-CHO,-OH,-COOH,-C=O四种形式存在,它们通常是活性炭吸附的活性中间点。pH值作为重要的介质因素,不仅仅影响吸附点解离,而且影响重金属离子的溶液化学水解,氧化还原反应和沉淀。了解到一般工业废水中重金属离子的平均浓度为60mg/L,而当重金属离子初始浓度为60ppm时,金属离子存在的pH范围为1~7,因此本实验选择在pH值3.0~6.5,结果如图1所示。
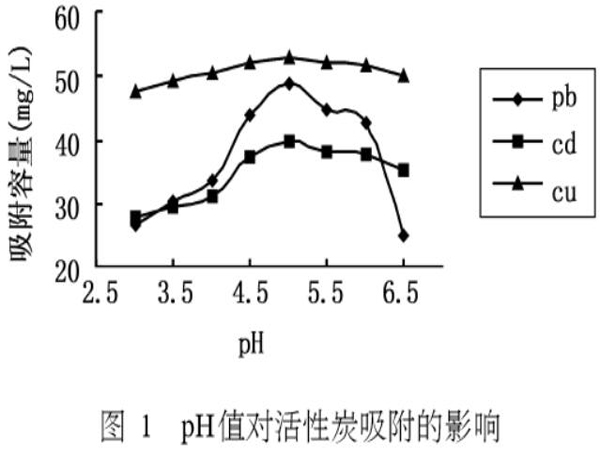
从图上可以看到当溶液的pH在3.0~6.5之间时,随着pH值升高,活性炭吸附容量升高,但是随着pH的继续升高,吸附容量反而降低。这是因为在pH值很小的时候,溶液中存在大量的H+离子,活性炭表面的-CHO、 -OH、-COOH、-C=O会跟溶液中的H+结合,改变了活性炭表面的亲和性,此时,活性炭的有效活性中间点被H+占据,重金属离子没有充分被吸附,所以吸附量相对较低。随着溶液的pH值的升高,跟活性炭表面官能团结合了的H+会发生离解,使得大量的活性中间点暴露在外面,重金属离子将占据这些活性中间点而有效地被吸附,所以吸附量是随着pH值的增加而加大的。但是随着pH值继续加大,溶液中的OH-与金属离子的化学作用力增加,导致吸附量的相对下降,因此本实验选择较佳pH值为4.8。
二、温度对活性炭吸附铅镉离子的影响
活性炭对重金属的吸附作用实际为吸附和脱附两个过程的竞争,一般吸附是放热过程,低温有利;而脱附是吸热过程,高温有利。本次模拟实验中固定其他条件(铅镉铜溶液100mL,pH4.8,初始浓度60 mg/L,活性炭用量0.3000g,恒温振荡2hrs),对20℃~70℃的吸附过程进行了考察,结果如图2所示。
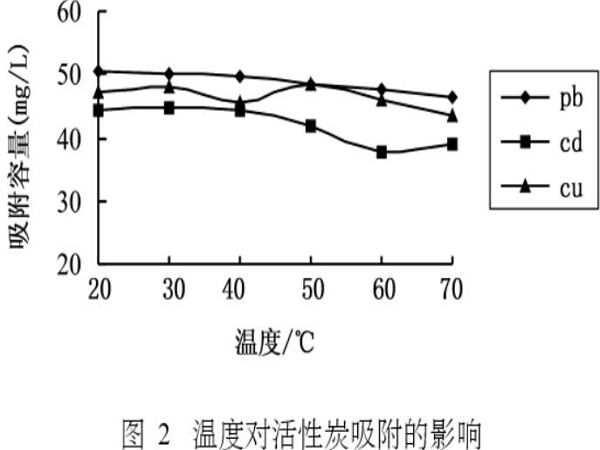
从图可以看出低温时温度对吸附容量影响不大,而且对重金属的吸附可达很好的效果。因此从微观的角度,温度主要是影响分子的布朗运动,而本实验所用的活性炭是中孔径的,能够很有效地吸附溶液中的金属离子,所以金属离子能够很好地进入活性炭的孔隙达到吸附平衡。而当溶液温度较高(高于50℃)时,液相吸附热虽然较小,但是由于分子热运动的加剧,导致对吸附平衡的破坏,吸附容量有所减小,表现为物理吸附性能的特性。因此本实验过程选择温度为室温25℃。从实验数据来看,重金属离子的吸附量波动变化不是很大,这说明自制活性炭适用于实际环境水样中重金属废水的处理。
三、活性炭用量对活性炭吸附铅镉离子的影响
对于相同的溶液,随着活性炭用量的增加,被吸附离子的相对浓度是降低的,吸附效果是增强的,但它的单位吸附量呈现减小的趋势,活性炭的用量对吸附有一定的影响,为了探索它的影响,我们恒定其他条件(铅镉铜溶液100mL,pH4.8,初始浓度60mg/L,恒定室温振荡2hrs),分别称取0.0500g,0.1000g,0.2000g,0.3000g的活性炭加入其中,分析结果见图3。
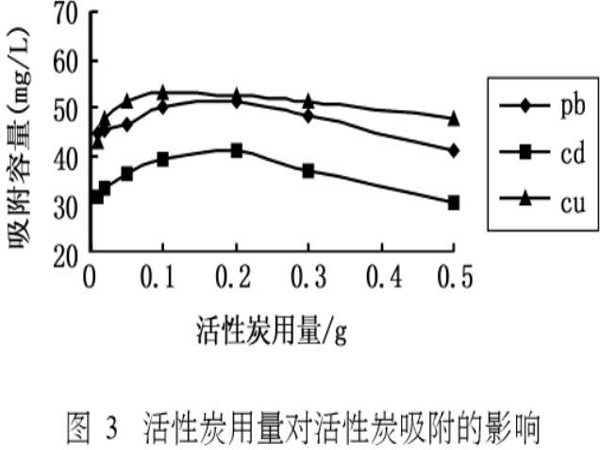
由图3可知,随着活性炭投加量的加大其对溶液中金属离子的吸附容量逐渐减少,对于相同投加量的活性炭对铜离子的吸附容量高,铅离子次之,镉离子少。对于一定浓度的铅镉铜离子来说,随着活性炭用量的增加,各种离子的吸附效率也随之增加,因为当原水中浓度一定时吸附剂量增加,可供吸附的活性位点增多,吸附剂上吸附的吸附质相对量增加,则达到吸附平衡时,吸附质的平衡浓度降低,因而吸附去除率升高,但吸附容量却随着吸附剂量增加而降低,其原因是吸附剂量增加,平衡浓度降低,单位吸附剂的相对吸附容量却随之下降。因此60mg/L的100ml溶液中,结合去除效果和吸附容量,活性炭的用量选择为0.2000g。
四、吸附时间对活性炭吸附铅镉离子的影响
在活性炭的吸附过程中,振荡时间对吸附效果也有较大的影响,溶液中的吸附质占据活性中间点是一个渐进的过程,即需要一定的时间来使吸附达到平衡,这一段时间即所谓的吸附平衡时间。只有达到了吸附平衡时间,活性炭才能较大限度的发挥效能。固定其他条件不变(铅镉铜溶液100mL,pH4.8,初始浓度60mg/L,活性炭用量0.2000g,恒定室温),分别振荡不同时间,结果见图4。
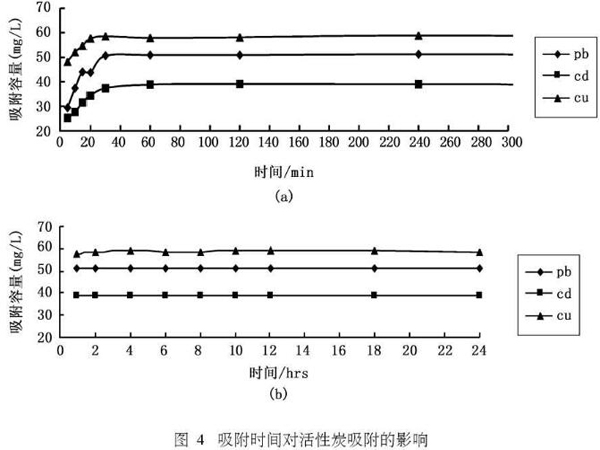
可以看出,三种重金属离子在活性炭上的吸附容量均随吸附时间的增加而增加,但当吸附时间达60min左右时则基本不变。开始时吸附容量上升很快是因为此时重金属离子在活性炭上的吸附主要发生在外表面上,随着吸附的进行,吸附质逐渐由大孔经过过渡孔深入到微孔中,重金属在内孔中传质速度逐渐减慢,吸附容量随时间缓慢增加,直至达到吸附平衡。因此,在静态吸附影响因素的实验中取振荡时间为60min,而在等温吸附实验中,为了确保吸附充分达到平衡,取振荡时间为24hrs。
五、吸附性能及机理分析
静态吸附容量也是描述和预测活性炭的吸附性能的重要指标,因此根据活性炭吸附前后样品浓度的变化,选用Freundlich模型和Langmuir模型来进一步分析其吸附性能。在室温的条件下,固定活性炭加入量0.2000g、pH4.8和震荡时间24hrs等条件,对一系列不同浓度的重金属离子进行吸附实验,测试在吸附平衡后相对应的溶液中金属离子浓度,所得数据换算为吸附量,分别绘制了铅镉铜的吸附等温线。铅镉铜金属离子在活性炭上的吸附行为遵循Langmuir公式,并且在所考察的浓度范围内,吸附行为又符合Freundlich方程。其相关参数见表1。
表1活性炭对重金属离子的吸附模型参数
| 重金属 | L | F | ||||
| Qm(mg/g) | b | R2 | K | 1/n | R2 | |
| 铅 | 52.54 | 0.148 | 0.9777 | 5.544 | 0.704 | 0.9931 |
| 镉 | 35.65 | 0.1092 | 0.9619 | 3.379 | 0.437 | 0.9695 |
| 铜 | 57.02 | 0.2418 | 0.9581 | 6.472 | 0.129 | 0.9778 |
R2相关系数,F型和L型拟合相关均达到0.95以上,表明活性炭对金属离子的吸附符合吸附等温方程。根据L型模型,Qm是理论饱和吸附容量,b是Langmuir常数,与吸附能量有关,是表征吸附能力的常数,因此活性炭对金属离子吸附容量和吸附能力大小顺序为Cu2+>Pb2+>Cd2+。分析F型模型,n大则吸附趋势大,即金属离子浓度对吸附的影响趋势是Cu2+>Cd2+>Pb2+;K值的大小可大致判断吸附能力的强弱,吸附能力是Cu2+>Pb2+>Cd2+,与L型类似。
六、结论
1、经过以上实验分析得出该活性炭吸附金属离子的较佳条件:100mL溶液较佳pH值4.8,活性炭的投加量0.2000g;吸附过程受温度影响不大,试验取室温;如果工艺流程要求快速有效,时间可设定为60min,如果静沉作为工艺流程之一,且要求高去除率,处理时间则设定为10~12小时。
2、吸附的机理一般为离子交换,化学反应吸附或捕集物理吸附,由于活性炭吸附可以用F型和L型模型进行较好的拟合,线性相关系数均在0.95以上,说明三种金属离子在活性炭上的吸附属单分子层吸附,该吸附过程属于物理吸附和化学吸附并存的物理运动过程,只要金属铅离子充分接触活性炭表面并进入空隙内部就能有效地被吸附,但当吸附到达一定的时间后,吸附运动基本达到一种动态平衡。
3、活性炭对Pb2+、Cd2+、Cu2+的较大吸附容量分别可达到52.54mg/g、35.65mg/g、57.05 mg/g;吸附能力大小顺序为Cu2+>Pb2+>Cd2+;金属离子浓度对吸附的影响趋势是Cu2+>Cd2+>Pb2+。
